Menu
Toxicologia
Os estudos não-clínicos de toxicologia têm como objetivo identificar e qualificar possíveis efeitos tóxicos de uma substância no organismo, bem como estabelecer uma dose inicial segura para a realização de testes em humanos. Embora também possam ser realizados de maneira exploratória, a conformidade destes ensaios com as Boas Práticas de Laboratório (BPL) é uma exigência regulatória para a autorização de estudos clínicos.


Toxicologia
Genotoxicidade
Ensaios disponíveis
Teste de mutação reversa em bactérias (teste de AMES), conforme o guia nº 471 da OECD.
Determinação de micronúcleos em células hematopoiéticas de camundongos (in vivo), conforme o guia nº 474 da OECD.
Testes de genotoxicidade são ensaios in vitro e in vivo concebidos para detectar compostos que induzem danos genéticos por diferentes mecanismos. No CIEnP, esses ensaios são realizados de acordo com as recomendações do guia ICH S2(R1) e em conformidade com as BPL.
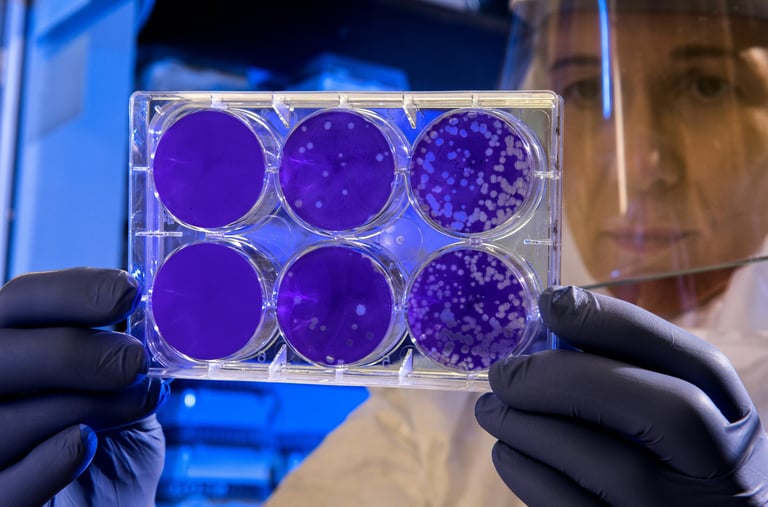
Toxicologia Geral
Ensaios disponíveis
Estudo de dose máxima tolerada (MTD);
Estudo de toxicidade oral de 14 dias
Estudo de toxicidade oral de doses repetidas de 28 dias (guia nº 407 da OECD; BPL)
Estudo de toxicidade oral de doses repetidas de 90 dias (guia nº 408 da OECD; BPL)
Estudo de toxicidade oral de doses repetidas de 180 dias (guia nº 452 da OECD; BPL)
Estudo de toxicidade oral de doses repetidas de 52 semanas (BPL)
Estudo de toxicidade parenteral aguda ou subcrõnica (BPL)
Estudo de toxicidade intranasal aguda ou subcrônica (BPL)
Estudo de toxicidade dérmica aguda ou subcrônica (guias nº 402 e 410 da OECD)
Estudo de toxicocinética (guia nº 417 da OECD)
Ensaio de tolerância local
Os estudos de toxicidade geral envolvem ensaios de toxicidade aguda, subaguda, subcrônica e crônica, que podem também ser subclassificados de acordo com a frequência de administração (dose única ou repetida) e objetivo da avaliação (toxicidade sistêmica ou local). O CIEnP realiza diversos estudos de toxicidade em ratos e camundongos e possui certificação em BPL para os principais deles.


Toxicologia Reprodutiva e do Desenvolvimento
Ensaios disponíveis
Estudo de fertilidade e desenvolvimento embrionário inicial
Estudo de desenvolvimento embriofetal
Os estudos de toxicidade reprodutiva e do desenvolvimento visam investigar possíveis efeitos de candidatos a medicamentos na reprodução e no desenvolvimento de mamíferos relevantes para a avaliação do risco humano. As investigações abrangem observações ao longo de um ciclo de vida completo (ou seja, desde a concepção em uma geração até a concepção na geração seguinte) e são realizados conforme orientações do guia S5 (R3) do ICH.


Pronto(a) para o próximo passo? Solicite um orçamento.
Veja outros serviços que podem ser do seu interesse.
Endereço
Av. Luiz Boiteaux Piazza, 1302 - Sapiens Parque, Cachoeira do Bom Jesus, Florianópolis, Santa Catarina, Brasil.
Segunda a sexta-feira das 08:00 às 17:00 horas.
©2024 - Centro de Inovação e Ensaios Pré-Clínicos
Mapa do site
Serviços
+55 (48) 3332-8400
contato@cienp.org.br
